從醫藥研發新政視角看醫藥產業趨勢
來源:解驕陽 瀏覽人數:19558 時間:2017/09/18
隨著我國經濟不斷發展、社會老齡化程度變高、疾病的慢性化特征越來越明顯,人民群眾對醫療健康的關注不斷增強,中國醫藥行業的需求持續增長。人的一生避免不了看病吃藥,我們每個人都受益醫藥產業的發展。從全球的發展趨勢可以看到,絕大多數國家的醫藥衛生費用支出占GDP的比例都是不斷提高的。醫藥市場的需求不僅隨著各國經濟發展而表現出持續繁榮,而且將超越經濟發展速度并呈現出開放式增長的特點。
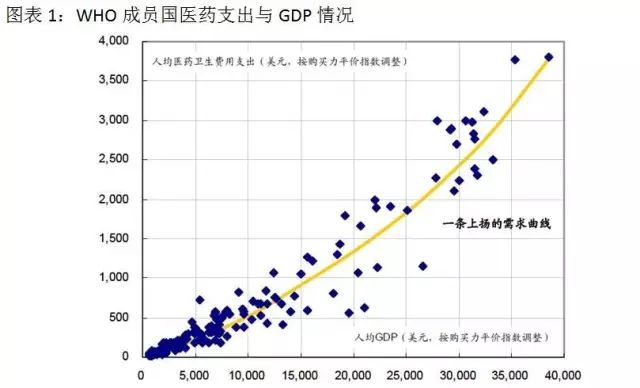
在長期看好醫藥產業發展的同時,我們也應該注意醫藥行業的特殊性。醫藥企業的下游主要是處于強勢地位的醫院等醫療機構,醫院和醫生很大程度上決定著患者最終醫藥消費。藥品市場本身是非常市場化的,但醫藥企業所面對的是非市場化的實體——強大的產業監管系統和支付方,政策對產業影響就變得至關重要。同時研發又是醫藥企業長期持續發展的核心競爭力,那么從與醫藥研發相關的新政策這個視角切入能較好的前瞻未來產業趨勢。
自2015年7月22日CFDA發布的“對1622個已申報生產或進口的待審藥品注冊申請開展藥物臨床試驗數據核查”文件至今,國務院、CFDA、CDE發布了一系列重磅政策,從藥品研發端鼓勵我國醫藥企業進行創新與國際接軌,這必將給產業帶來深遠影響和很好的投資機會。這些政策主要包括臨床數據核查、集中審評、優先審評審批、仿制藥一致性評價、化學藥品注冊分類改革和上市許可持有人試點等。
臨床試驗數據自查核查是新政開端,目前已經常態化。臨床數據核查按照“最嚴謹標準、最嚴格監管、最嚴厲處罰、最嚴肅問責”的要求,建立長效工作機制,確保藥物臨床試驗數據真實可靠。數據核查開展的初衷是在審藥品大量積壓,阻礙了藥品審批進度。此外,國家開展臨床數據核查,可以獲得更有效真實的臨床數據,有利于患者和整個醫藥產業的長遠發展。從目前的效果來看,臨床數據核查帶來大規模的撤回緩解了積壓,將壓縮仿制藥的低水平仿制,能使審評重點轉移到創新上,優化資源配置。
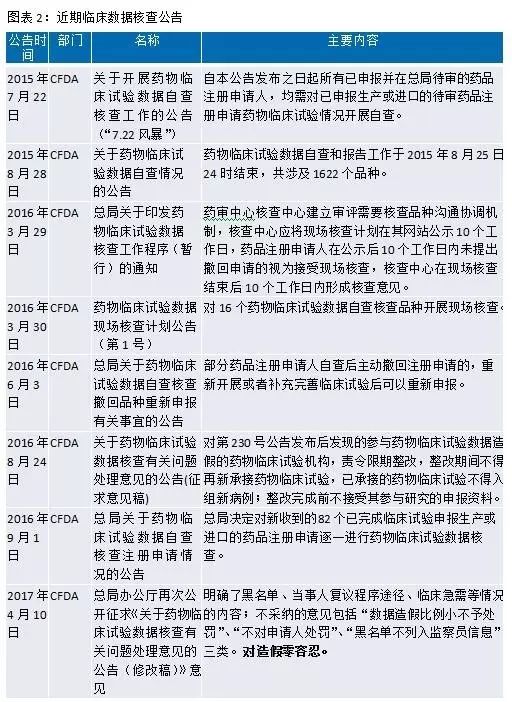
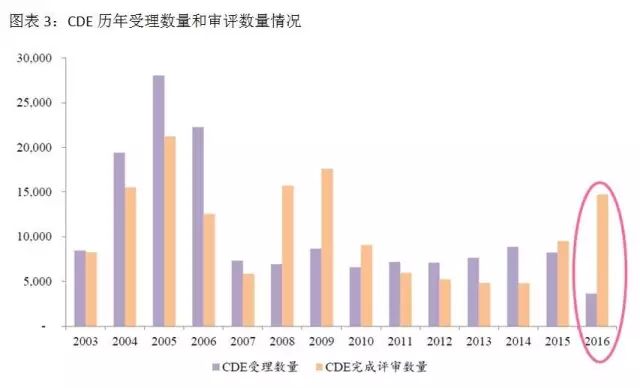
2016年2月26日,CFDA發布《關于解決藥品注冊申請積壓實行優先審評審批的意見》,把重大疾病用藥、創新藥、優質仿制藥、市場短缺藥物納入優先審評審批的范疇。在藥品審評審批改革前,有近一半的時間是在CDE排隊等待。
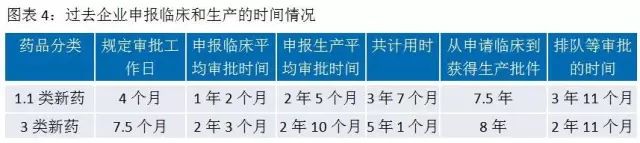
開展優先審評審批以后,納入優先審評審批序列的藥品,CDE每隔一個月會發布一批品種名單,列入優先審評的申請不再排隊直接啟動審評。其中對于新藥的臨床試驗申請和生產注冊申請的各個環節所需時間進行了詳細規定,新藥的審評審批時間得以大幅壓縮。

由于創新藥的臨床普遍比仿制藥更規范和受益于優先審評審批政策,近兩年批準臨床的批件創歷史新高。1.1類新藥審批大量增加,新藥放量趨勢開始出現。未來會有更多的創新藥和優質仿制藥受益于優先審評審批,促進我國醫藥企業的創新升級。
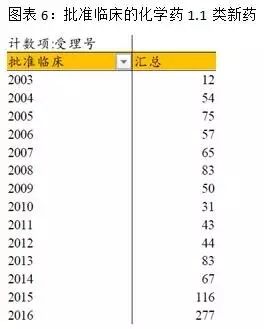
國內已經有部分藥企的產品通過FDA、歐盟的質量認證,近年來國內的仿制藥水平受到國際上的一定認可。但是總體來說,國內的化藥仿制藥與原研產品在產品有效性、安全性上還有一定差距。從深化醫改和醫保控費的趨勢下,進口替代勢在必行,而一致性評價又是實現進口替代的藥品質量保證。近期CFDA關于一致性評價政策的密集出臺,最新的是2017年9月4日CDE發布《關于公開征求<中國上市藥品目錄集>框架意見的通知》,作為落實一致性評價工作的重要舉措,這一中國版“OrangeBook”的制定進入起步階段。
一致性評價對患者而言能保證用藥安全,降低醫療費用;對制藥企業而言,能提高用藥質量,減少無序競爭;對醫藥行業而言,能提高整體水平,具有國際競爭力。此外,一致性評價在支付端能享有招標單獨分組、按品種設定醫保支付標準、優先選用通過品種等政策扶持。
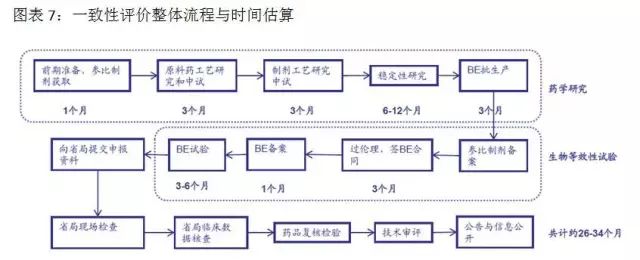
一致性評價研究耗時時間長、投入多、難度大。對于企業來說,難度主要體現在:參比制劑的確定與獲取、處方工藝的研究、生物等效試驗的不確定性。一個品種完成一致性評價,費用約500-800萬元,耗時32-36個月。其中藥學研究和二次開發花費約占一半,生物等效性試驗花費約占一半。資金充裕、研發實力雄厚的大型藥企會有選擇的進行一致性評價研究,中小型制藥企業將主要精力用于市場領先的、收入占比大的品種優先一致性評價工作,競爭力弱的相關品種直接放棄。目前一致性評價進度低于預期,但從長期來看,必將促進行業的健康發展。
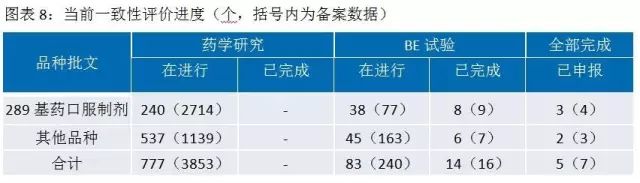
此外,國務院、CFDA等還出臺了許多配套政策來提高我國藥品質量,促進醫藥行業研發創新。例如MAH(藥品上市許可持有人制度)表明藥品所有權屬于研發公司或者個人,國家通過這個制度,鼓勵創新,激勵研發人員,有利于創新產品開發;對化藥注冊分類進行改革,定義更嚴格,更強調臨床價值,鼓勵真正的創新等。
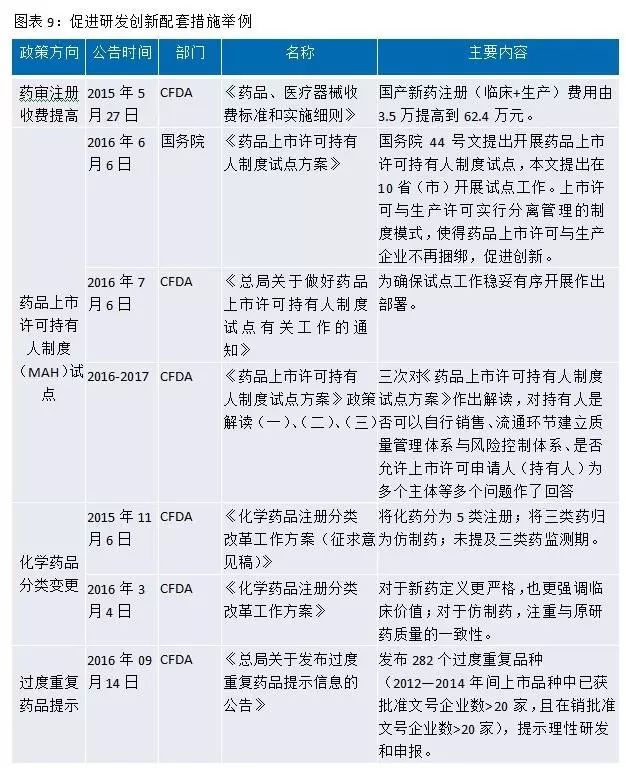
從政策的不斷出臺和落地來看,國家對醫藥研發端的創新升級可謂非常重視,速度和力度超越市場預期。新的政策給醫藥行業即帶來挑戰又帶來機會,減少了注冊積壓,加快了審評,加快了與國際接軌,鼓勵優勝劣汰,鼓勵創新。當今中國醫藥行業正處于大的變革,研發越來越成為醫藥企業的核心。從世界制藥發展史來看,世界級大型制藥企業基本上都是研發型藥企,多來自藥品監管相對寬松的國家,比較從容的市場環境使制藥企業能夠以研發為根本追求企業的長期可持續發展。1891年美國默克成立,從默默無名的小公司開始一步步成為世界制藥巨頭,其發展歷程值得我們去思考和學習。《制藥世家默克》一書中也曾寫到“制藥業是那么的反復無常。一切取決于下一步的試驗結果,或者是食品和藥品管理局的一道命令,或者是默克新的降脂藥或宮頸癌疫苗。但公司堅信,公司在2003年的利潤增長會重新達到兩位數。而最關鍵的是,默克實驗室是否聚集了具有研發能力的精英,以及公司是否有東山再起的激情,不管怎樣,研發和人還是制藥企業的根本所在。”醫藥企業雖然永遠受到行業政策和監管的影響,但那些立志要滿足人類對健康和生命無止境追求的優秀醫藥企業們,必將通過不斷研發創新來發展壯大并改變世界。縱觀海外發達市場走過的道路,有理由相信我們正走在一條正確的道路上,我國優秀醫藥企業將抓住產業的變革,立足研發,走向世界,改變人類。

 粵公網安備 44030402005514號
粵公網安備 44030402005514號